adenozin
adenosine
az adenin (→purinbázis) és a ribóz egyesüléséből keletkező nukleozid; a dezoxiribóz és az adenin kötödéséből a dezoxiadenozin keletkezik. Az adenozin származékai fontos biológiai molekulák. Foszfát származékai nukleotidok (AMP, ADP, ATP, cAMP) – ezek minden sejtben jelen vannak, az ATP a legnagyobb mennyiségben. (A dezoxiadenozin nem képezi ezeket.)
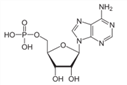
▪AMP (adenozin-monofoszfát) az adenin és ribóz alkotta adenozin és egy foszfát egyesüléséből jön létre – nevezik adenilsavnak is. Az RNS egyik nukleotidja. Az adenin, a dezoxiribóz és foszfát kötődéséből a dezoxiadenozin-monofoszfát (dAMP) keletkezik, ez a DNS alkotóeleme. (→DNS, RNS) A foszfát (PO4) észterkötéssel kapcsolódik a szénhidrát egyik alkoholos hidroxilcsoportjához (OH–CH3), szokásosan az 5’-szénatomhoz (AMP néven mindig ezt értjük, a kötődés helyét nem jelöljük). Kötődhet azonban a szénhidrát 4’-, 3’- és 2’-szénatomán található hidroxilcsoporthoz is, többféle azonmás keletkezhet (ezekben jelöljük a kötődés helyét). Ha egy foszfátcsoport ugyanazon adenozin két hidroxilcsoportjához (az 5’ és 3’ csoportokhoz) kapcsolódik, gyűrűs szerkezet (cyclic AMP, cAMP) alakul ki.
▪ ADP (adenozin-difoszfát) az AMP-ből foszfát felvételével képződik. Az első foszfát (α-foszfát) észterkötéssel kapcsolódik a ribózhoz/dezoxiribózhoz, a második (β-foszfát) az α-foszfáthoz nagyenergiájú foszfoanhidrid-kötéssel.
▪ ATP (adenozin-trifoszfát) az egyik legjelentősebb energiahordozó molekula; az adenozin és három (α, β, γ) foszfát egyesüléséből jön létre. Az energiát az első és második, illetve a második és harmadik foszfátcsoport közötti kötésben tárolja. Energia leadásakor, ha az utolsó (γ-helyzetű) foszfát hasad le vízbontással, akkor ADP és foszfát; ha az első és második foszfát között szakad fel a kötés: AMP és pirofoszfát (PP, kettősfoszfát) keletkezik, és energia szabadul fel; ez a sejtek működésének az alapvető energiaforrása.
Az ATP – szemben az AMP-vel – a hőegyensúly szempontjából nem tartós szerkezetű molekula, ezért könnyen megszabadulna a γ-helyzetű foszfátjától, de megválna a β-helyzetűtől is, hogy szerkezete kiegyensúlyozott legyen. Önmagától azonban erre még víz jelenlétében is csak nagyon kis eséllyel képes: a bontáshoz szükséges vízmolekula nehezen tud bekötni a megfelelő helyre. A foszfátleadás ezért hatékonyan csak enzimek közreműködésével megy végbe. Az enzim a folyamatban állványként szolgál, kapcsolja az ATP-t, és felszínén megfelelő helyzetben köti meg a vizet a foszfoanhidrid kötés felbontásához.
• cAMP (cyclic AMP, gyűrűs AMP) köztijel (intermedier mediátor) a G-fehérje-kapcsolt jelfogóval társult többféle jelközvetítésben; a sejtplazma állandó összetevője. A G-fehérje serkentő hatására a sejthártya belfelszínén vagy sejtszervecske felszínén található adenilát-cikláz (adenylyl cyclase, adenyl cyclase, adenylate cyclase, AC) hozza létre ATP-ből. Az adenilát-cikláz bontja az ATP-t: lehasítja a β és a γ helyzetű foszfátját, amely pirofoszfátként (PP) lép ki a folyamatból, miközben gyűrűs AMP (cAMP) keletkezik. Ezzel szemben a ciklikus nukleotid foszfodiészteráz felszakítja a cAMP gyűrűjét a foszfát és a 3’ szénatom közötti kötésnél, „kiegyenesíti” a molekulát. Az adenilát-cikláz és a ciklikus foszfodiészteráz együtt szabályozza a cAMP töménységét a sejtplazmában, de sok más molekula is befolyásolja azt. A cAMP jelközvetítőket tevősít, köztük a fehérjekináz-A-t. Részt vesz az anyagcsere-folyamatok, a sejtburjánzás, a szövetfejlődés, a génátírás stb. szabályozásában; enzimek vagy más fehérjék serkentésével.
